Les morsures de serpent constituent un problème majeur de santé publique. Elles ont été reconnues comme maladie tropicale négligée prioritaire par l’Organisation mondiale de la Santé en 2017 (1). On estime plusieurs millions de cas annuels dans le monde, avec une mortalité et une morbidité importantes, principalement liées aux formes graves non prises en charge précocement (2,3).
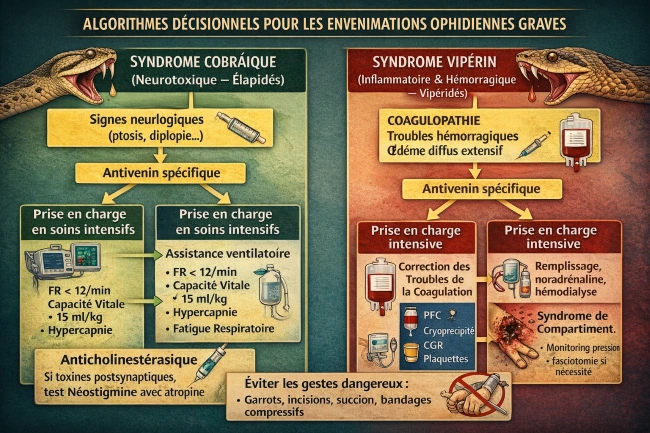
Deux syndromes dominent les tableaux cliniques sévères :
- Le syndrome cobraïque (neurotoxique)
- Le syndrome vipérin (inflammatoire et hémorragique)
1. Syndrome cobraïque (neurotoxique – Élpidés)
1.1 Physiopathologie
Les venins d’Élapidés contiennent des neurotoxines agissant à la jonction neuromusculaire (2,4).
Les neurotoxines postsynaptiques :
- bloquent les récepteurs nicotiniques de l’acétylcholine ;
- entraînent une paralysie flasque réversible.
Les neurotoxines présynaptiques :
- inhibent la libération d’acétylcholine ;
- provoquent une atteinte plus prolongée, parfois irréversible à court terme.
La conséquence est une paralysie descendante progressive pouvant évoluer vers une insuffisance respiratoire aiguë.
1.2 Signes cliniques
Les premiers signes sont : ptosis bilatéral (signe précoce majeur), diplopie, dysarthrie (difficulté d'élocution) et dysphagie.
L’évolution peut conduire à :
- Paralysie bulbaire (paralysie progressive des muscles de la bouche, de la langue, du pharynx et du larynx, provoquant des troubles de l'élocution, de la déglutition et de la mastication)
- Faiblesse cervicale (douleur de la nuque)
- Paralysie respiratoire
La conscience reste conservée.
1.3 Prise en charge des formes graves
1.3.1 Surveillance et réanimation
L’hospitalisation en unité de soins intensifs est indiquée en cas d’atteinte neurologique évolutive.
Indications d’intubation :
- Fréquence respiratoire < 12/min
- Capacité vitale < 15 ml/kg
- Hypercapnie
- Troubles de déglutition
La ventilation mécanique peut être nécessaire plusieurs jours (2,4).
1.3.2 Antivenin
L’antivenin doit être administré dès apparition de signes neurologiques (1,2). Il neutralise le venin circulant, limite la progression, mais n’inverse pas toujours immédiatement une paralysie constituée.
1.3.3 Anticholinestérasiques
Un test à la néostigmine peut être réalisé en cas de suspicion d’atteinte postsynaptique (4), sous atropine et surveillance cardiaque.
2. Syndrome vipérin (inflammatoire et hémorragique – Vipéridés)
2.1 Physiopathologie
Les venins vipérins contiennent plusieurs substances : Métalloprotéinases, Procoagulants, Phospholipases A2, Toxines cytotoxiques. Ils induisent :
- Œdème inflammatoire massif
- Nécrose locale et parfois gangrène
- Coagulopathie de consommation (CIVD)
- Dysfonction endothéliale
- Insuffisance rénale aiguë (2,3)
La CIVD se distingue dans ce contexte par l’absence fréquente de microthromboses diffuses (3).
2.2 Signes cliniques
- Locaux : Douleur intense, Œdème extensif, Phlyctènes, Nécrose
- Systémiques : Hémorragies muqueuses, Hématurie, Hémorragies digestives, Hypotension, Insuffisance rénale aiguë
- Biologie : TP effondré, TCA allongé, Fibrinogène bas, Thrombocytopénie
3. Prise en charge hospitalière des formes graves vipérines
3.1 Antivenin
Les antivenins (ou sérums antivenimeux) sont des préparations d’immunoglobulines spécifiques obtenues après immunisation d’animaux (le plus souvent chevaux ou moutons) par des doses croissantes de venin. Les anticorps produits sont ensuite purifiés pour neutraliser les toxines circulantes.
L’antivenin n’inverse pas immédiatement les lésions tissulaires déjà constituées, mais empêche la progression de l’envenimation.
L’OMS recommande de ne pas retarder l’administration en cas d’envenimation systémique avérée.
C'est le traitement spécifique central (1,2). Ses indications sont :
- Coagulopathie
- Hémorragie active
- Extension rapide de l’œdème
- Défaillance d’organe
Administration IV lente après dilution, sous surveillance continue. La dose dépend de la quantité de venin injectée et non du poids du patient.
Réactions indésirables : risque d'allergie, Adrénaline toujours à portée.
3.2 Correction des troubles de la coagulation
Les produits sanguins ne doivent être administrés qu’après neutralisation du venin (3). Indications :
- Plasma frais congelé si hémorragie active
- Cryoprécipité si fibrinogène < 1 g/L
- Plaquettes si thrombocytopénie + saignement
- Concentrés globulaires si anémie sévère
Surveillance biologique toutes les 4–6 heures initialement.
Les produits sanguins ne doivent être administrés qu'après antivenin, en cas d’hémorragie active ou en cas de geste invasif urgent.
Produits utilisés :
| Situation | Produit recommandé |
| Fibrinogène < 1 g/L + saignement | Cryoprécipité ou fibrinogène concentré |
| TP très bas + hémorragie | Plasma frais congelé |
| Thrombocytopénie sévère + saignement | Concentrés plaquettaires |
| Anémie sévère | Culots globulaires |
⚠️ L’administration isolée de plasma avant antivenin est inefficace.
3.3 Prise en charge du choc
- Remplissage vasculaire
- Vasopresseurs (noradrénaline)
- Surveillance hémodynamique
3.4 Insuffisance rénale aiguë
- Mécanismes : Hypoperfusion, Hémolyse, Myolyse, Microangiopathie
- Traitement : optimisation hémodynamique, épuration extra-rénale si critères habituels
Discussion
Les formes graves d’envenimations ophidiennes relèvent pleinement de la médecine d’urgence et de la réanimation.
Le pronostic dépend de la précocité d’administration de l’antivenin (1,2), de l’accès à la ventilation mécanique et de la correction rapide des troubles hémodynamiques et hémostatiques
Une prise en charge protocolisée améliore significativement la survie (2–4).
Conclusion
Le syndrome cobraïque expose à une défaillance respiratoire aiguë nécessitant une assistance ventilatoire précoce.
Le syndrome vipérin expose à une coagulopathie sévère et à des complications hémorragiques et rénales.
L’antivenin demeure le traitement spécifique central, associé à une réanimation adaptée.
Lisez notre article en rapport : Morsure de serpent, physiopathologie et CAT
Références
- Organisation mondiale de la Santé. Guidelines for the management of snakebites. 2nd ed. Geneva: WHO; 2016.
- Gutiérrez JM, Burnouf T, Harrison RA, et al. Snakebite envenoming. Nat Rev Dis Primers. 2017;3:17063.
- Isbister GK, et al. Snakebite. Lancet. 2018;392:109–121.
- Warrell DA. Snake bite. Lancet. 2010;375:77–88.
®2026 - efurgences.net


